- 时间点:
- 时 分 秒 当前视频时间点
- 问题:
-
- 选项一
设为正确答案
新增选项 - 选项一
- 正确跳转时间:
- 时 分 秒 同锚点时间
- 错误跳转时间:
- 时 分 秒 同锚点时间




恭喜你,回答正确~
很遗憾,回答错误~
正确答案: ,您可以



本课为第二单元课题1空气第一课时的教学内容,空气是人人都离不开的最重要的化学物质,由于看不见,摸不着,学生只知道其重要,却不十分清楚空气到底是什么。空气对学生来说是一种非常熟悉的气体,教材选择了空气作为初中化学中接触物质知识的开端,不仅承接了小学对空气知识的介绍,更重要的是它与人类的生活关系最为密切,是人类不可离开的天然物质,同时氧是化学性质比较活泼的元素,通过对它的认识和了解,可以比较顺利地引导学生进入化学世界来探索物质的奥秘。而且,选择以空气为主题,开始这一单元的教学活动,是符合“从学生熟悉的事物入手,进行科学教育”的原则。然而学生刚开始学化学,虽在绪言和实验基本操作课上了解掌握了一些知识和操作,但相应的知识储备也是相当不足的,比如C、S、P等物质燃烧后的产物和状态他们都还没有学到;还可能大多数学生对气体减少压强降低的物理原理也不知道,所以要引导他们完成对空气成分的探究是有一定的困难。但我们可以从看图了解拉瓦锡研究空气成分开始,先对气体减少压强降低的物理原理进行解释,然后再到做仿照实验来测定空气里氧气的含量,再引出混合物和纯净物的概念,最后到看图片认识空气的主要用途和保护空气,其实可以说教材是深入浅出,也为我们以后的学习提供一个合理的思维方式。通过本课题的学习,使学生又一次认识到生活中的自然科学知识,进一步激了学生学习自然科学的兴趣。
初中生在学习化学之前,对空气和氧气都有一定的常识,但是比较零碎、不够深入,对一些实验的基本操作和知识不够了解,但可以用身边的小实验让学生感受空气的存在来激发学生学习的兴趣和好奇心。初中生有着基本的辨别是非的能力及环境忧患意识,从周围环境的污染和恶化让学生意识到保护空气的重要性。
知识与技能
1、了解空气的主要成分
2、初步认识纯净物、混合物的概念,能区分一些常见的混合物和纯净物
过程与方法
1、通过对“测定空气里氧气的含量”实验的操作,分析空气的组成
2、通过对常见物质的比较,了解混合物和纯净物的概念
情感、态度与价值观
1、知道空气是一种宝贵的自然资源
2、养成关注环境,热爱自然的情感
重点
1、了解空气的组成,各成分用途
2、认识纯净物、混合物的概念,并能区分常见的混合物和纯净物
难点
如何指导学生观察及描述实验现象
课题1 空气
一、空气中氧气含量的测定
1、装置
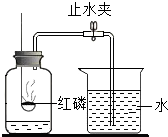
原理:红磷 + 氧气![]() 五氧化二磷
五氧化二磷
现象:红磷燃烧,冒出大量白烟 ,放出热量,水倒流入集气瓶,约占瓶内原空气体积的1/5
结论:氧气约占空气总体积的1/5
2、空气的组成
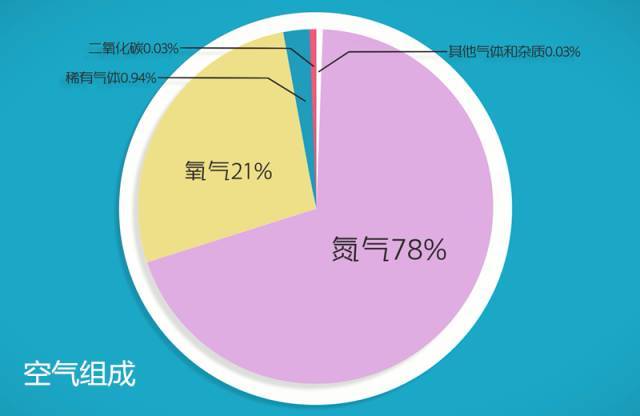
巧记:氮七八、氧二一,零点九四是稀气,体积分数要牢记
3、物质的分类
纯净物:由一种物质组成
混合物:由两种或两种以上物质组成
教学过程
[导入新课]
举例验证空气的存在;感受空气的存在。(用空集气瓶在盛满水的水槽中向下压、注射器实验来证明空气的存在。)今天我们就来学习有关空气的知识。
[推进新课]
[过渡]因为空气是一种无色、无味的气体,所以人们对空气的认识比较晚。17世纪中叶以前,人们一直认为空气是一种单一成分的物质,直到18世纪,通过对燃烧现象和呼吸作用的深入研究,人们才开始认识到气体的多样性和空气的复杂性。
一、空气是由什么组成的
[分析]为了搞清楚空气的成分,很多科学家致力于这方面的研究,如瑞典化学家舍勒和英国化学家普里斯特里.其中最有名的就是法国化学家拉瓦锡做的实验.[图片展示]
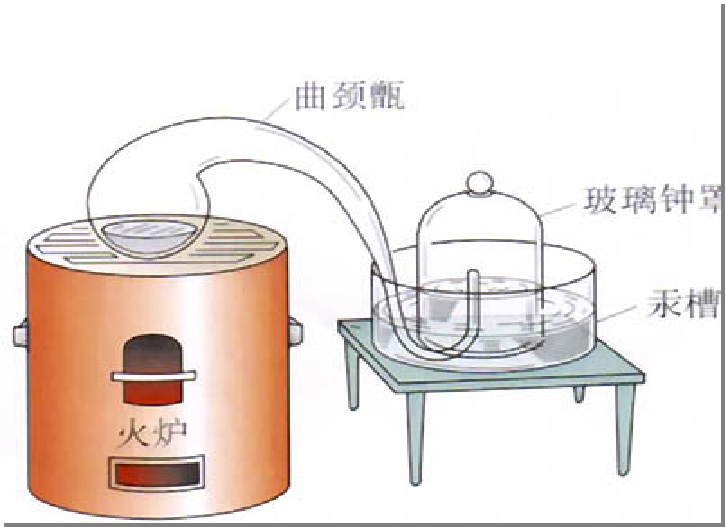
研究空气成分的装置
[分析]拉瓦锡,他最早运用天平作为研究工具,用液态的金属汞作为研究对象,经过大量实验最终研究出了空气的成分,得出了结论:空气是由氧气和氮气组成的。氧气约占空气总体积的1/5。
[过渡]拉瓦锡的实验是在200多年前做的,由于受到当时条件的限制,他的实验比较麻烦。现在我们已经能用简单的实验来验证拉瓦锡所得出的结论,接下来我们就用红磷做原料来测定一下空气中氧气的含量。
[实验] 实验步骤: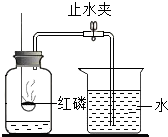
1.连接仪器,检查装置气密性。
2.在集气瓶内装有少量的水,并将水面上方空间分为5等份。然后再用弹簧夹夹紧胶皮管。
3.点燃燃烧匙内红磷,立即伸入瓶中,塞紧胶塞。
4.待集气瓶冷却到常温时,打开弹簧夹。
现象:
1、红磷燃烧有黄色火焰产生大量白烟(固体小颗粒),放出热量。
2、水倒流入集气瓶,约占瓶内原空气体积的1/5。
[实验原理解释]:
足量的红磷燃烧后,耗尽了集气瓶中的氧气,生成固体五氧化二磷;燃烧停止,温度降低后,瓶内压强减小;当打开弹簧夹时,烧杯中的水在大气作用下,流进集气瓶,增补了空气中氧气的体积。
[过渡]在红磷燃烧这个实验中,红磷与空气中的氧气反应,生成了一种叫做五氧化二磷的白色固体,我们可以用文字的形式把这个反应表示出来:红磷+氧气![]() 五氧化二磷
五氧化二磷
[结论]:氧气约占空气总体积的1/5
[讨论1]
1.在实验中如果进入水的体积小于集气瓶总体积的1/5,会是什么原因呢?
2.在进行该实验时,如果深入燃着的红磷速度太慢,会造成什么后果呢?(热胀冷缩)
3.在进行该实验时,红磷燃烧时弹簧夹没有夹紧,会造成什么后果呢?(热胀冷缩)
[分析]学生讨论后再分析和总结实验成功的关键点
[讨论2]能不能把红磷用铁和木炭代替?
[分析]铁不能代替红磷。原因:铁不能在空气中燃烧,瓶内氧气的体积几乎不会变化。木炭不能代替红磷。原因:木炭燃烧后生成的二氧化碳为气体,集气瓶内气体压强基本不变。
[讲解]随着科学技术的不断发展和实验仪器的不断精密化,空气中的其他成分也被科学家通过实验一一发现。实验表明:
[讲解并板书]空气的成分按体积计算,大约是:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。
学生巧记:氮七八、氧二一,零点九四是稀气,体积分数要牢记
二、纯净物和混合物
[过渡]空气是由多种成分组成的,我们把它叫做混合物。而空气中的氮气或氧气都只由一种物质组成,我们把它们叫做纯净物。
[板书]纯净物和混合物
[分析]纯净物可以用专门的化学符号表示。如氧气:O2、氮气:N2、红磷:P、五氧化二磷:P2O5。
[师]根据你的理解,你能以纯净物和混合物的分类方法来区分黑板上的例子吗?
[学生举例、教师评价]
[师]通过刚才的学习,我们可以这样来表示纯净物和混合物。
[讲解并板书]
纯净物:由一种物质组成(可用专门的化学符号表示)。
混合物:由两种或多种物质混合而成(没有专门的化学符号表示)。
[补充]纯净物有固定的组成,混合物没有固定的组成。组成混合物的各物质之间不发生化学反应,它们各自保持各自的性质。如空气中的氧气和氮气就各自保持了自己的性质。
[巩固练习]
1.某同学利用如图装置测定空气中氧气的含量,红磷燃烧后恢复到室温,打开弹簧夹,发现进入广口瓶的水超过广口瓶容积的1/5。造成这一现象的原因可能是( )
A、实验前没有将弹簧夹夹紧 B、装置可能漏气
C、实验中所取的红磷过量 D、实验中所取的红磷不足
2.下列事实说明空气中含有哪些成分?
(1) 澄清的石灰水敞口放置在空气中会变浑浊【 】
(2) 小白鼠在装有空气的密闭容器中可存活一段时间【 】
3.判断下列物质那些是纯净物那些是混合物
1.清澈的河水 2.王老吉凉茶
3.氮气 4.洁净的空气 5.液氧
6.“统一”鲜橙多 7.冰水混合物
8.雪碧 9.二氧化碳
混合物是: .
纯净物是: .
[自主总结 ]
学生按照板书内容总结本节课所学内容,引导学生通过观察实验,研究实验,分析实验,从而掌握实验探究的真谛!
[作业布置]:
1.课后习题32页 1.2.3题
2.预习第二课时内容,并搜集有关O2、N2用途
[板书设计]
2.1.1空气是由什么组成的
一、测定空气中氧气含量
实验原理:红磷+氧气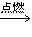 五氧化二磷
五氧化二磷
P O2 P2O5
实验现象:1、红磷燃烧有黄色火焰产生大量白烟,放出热量。
2、打开止水夹,烧杯中的水进入到集气瓶中,约占集气瓶体积的1/5。
实验结论:氧气约占空气体积的1/5。
二、空气的成分
按体积计算:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%
三、物质分类
纯净物:只有一种物质组成。
混合物:由两种或两种以上的物质混合而成的物质。
设为正确答案