- 时间点:
- 时 分 秒 当前视频时间点
- 问题:
-
- 选项一
设为正确答案
新增选项 - 选项一
- 正确跳转时间:
- 时 分 秒 同锚点时间
- 错误跳转时间:
- 时 分 秒 同锚点时间




恭喜你,回答正确~
很遗憾,回答错误~
正确答案: ,您可以



本节课内容选自高中化学人教版选择性必修一《化学反应原理》的第四章第一节。在化学必修2的第二章第二节《化学能与电能》的学习过程中,学生已初步掌握将化学能转化为电能的途径,并已初步具有原电池、正极、负极、电解质溶液的概念认识。本节将从概念建构的层面和定量分析的角度比较系统介绍原电池的组成和工作原理,并且能对常见的原电池现象进行解释,为电解池的学习做铺垫,在原有知识的基础上起到一个承前启后的作用,它是电化学学习的基础内容也是核心内容,在本章的学习中占有重要的地位,也与生活生产、科技前沿紧密相连。学习本节内容,既可以加深对氧化还原理论的理解,又加深学生对电化学反应所遵循规律的了解;本节设计了一些创新实验和科学探究活动,与信息技术有效结合,有利于学生增强探索化学反应原理的兴趣。
学生在高一掌握了氧化还原理论、金属活动顺序以及物理学中的电学知识。经过高一《化学能与电能》的学习,已经初步了解了原电池的原理,本节课内容对于学生而言是加深,因此设计探究环节,让学生自己得出相关结论。高二学生具备设计简单化学实验方案的能力,但创新思维还不成熟,缺乏多角度的综合分析能力。所以在实验设计部分不能完全交给学生自己想,为了使课程更加高效,应该多搭梯子,多给学生一些图片和已知信息给与一定的提示。特别是本次的教学对象是选择了化学科目的学生,他们在高一对化学是充满兴趣的,进入高二以来,难度加大,部分学生有些打退堂鼓,这节课可以重新树立学生对化学学习的信心和兴趣。
教学目标:
(1)通过复习回顾,认识原电池的组成条件,建立原电池装置的认识模型。
(2)通过从单液原电池到双液原电池的学习认识盐桥、离子交换膜的作用,掌握原电池的工作原理、能准确判断离子移动方向,正确书写电极反应式,能设计原电池。
(3)通过原电池装置优化探究过程,感受原电池的价值,了解化学在生产生活中的应用,培养可持续发展的意识,增强社会责任感,
评价目标:
(1)通过复习回顾和新课讲授,诊断并发展学生对原电池的组成条件及其工作原理(经验水平、概念原理水平)。
(2)通过分析单液原电池的弊端并提出改进措施,诊断并发展学生对原电池的认识进阶(宏观水平、微观水平、内涵水平)
(3)通过对原电池装置优化探究过程,诊断并发展学生的认识思路结构化水平(视角水平、内涵水平)和学生对化学价值的认识水平(学科和社会价值视角)。通过对学生实验操作的评价,诊断并发展学生实验操作水平。
教学重点:原电池的原理及相关应用
教学难点:以原电池原理来设计更好的原电池
原电池的工作原理
原电池:化学能转化为电能的装置
原电池的构成条件:两极、一液、一线、一反应
原电池的原理:
【创设情境】播放“美国特斯拉电动跑车”视频
介绍风靡全球的特斯拉电动跑车的优良性能,与其电池的性能是离不开的。
导入我们的课程类型是试验探究课,今天我们要一起来学习“原电池实验的高效化与微型化创新改进”
1.原电池的概念
教学目标:
(1)通过复习回顾,认识原电池的组成条件,建立原电池装置的认识模型。
评价目标:
(1)通过复习回顾和新课讲授,诊断并发展学生对原电池的组成条件及其工作原理(经验水平、概念原理水平)。
【回顾概念】原电池是将化学能转化为电能的装置。
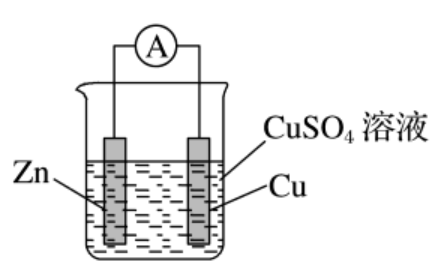
【设疑】我们知道,将锌片、铜片置于硫酸铜溶液中并以导线连接起来组成原电池。可以获得电流,然而这种原电池中氧化反应与还原反应并没有完全隔开,我们如何进行改进呢?
【实验】教师演示实验4-1,学生试观察现象。
【回答】
实验装置 |
装置一 |
装置二 |
|
实验现象 |
电流表 |
指针偏转 |
指针偏转;取出盐桥,电流表的指针回到零点 |
电极变化 |
锌片逐渐溶解,铜片上有红色固体生成 |
①左边烧杯中的锌片逐渐溶解,右边烧杯中的铜片上有红色固体析出 ②取出盐桥,铜片上不再有固体析出,锌片上也不再溶解 |
|
电流变化 |
一段时间后,电流会逐渐衰弱 |
产生的电流持续、稳定 |
|
【思考与交流】 1.盐桥的作用是什么?2.为什么装置一电流逐渐衰弱,装置二电流持续、稳定?
【讲解】带着问题,我们一起来分析原电池的工作原理。在盐桥存在时,在ZnSO4溶液中,锌片逐渐溶解,即Zn被氧化,Zn失去电子,生成Zn2+进入溶液。Zn失去的电子,经导线流向铜片,CuSO4溶液中的Cu2+从铜片上得到电子,被还原为金属铜并沉积在铜片上。随着反应的进行,左边烧杯溶液中c(Zn2+)增大,右边烧杯溶液中c(Cu2+)减小。盐桥中的Cl-移向ZnSO4溶液,K+移向CuSO4溶液,使左、右烧杯中的溶液均保持电中性,氧化还原反应得以持续进行,从而原电池不断地产生电流。
【思考】试分析取出盐桥后电流表的指针回到零点的原因。
【回答】取出盐桥后,由于锌原子失去电子成为Zn2+进入溶液,使ZnSO4溶液因Zn2+增多而带正电;同时Cu2+得到电子成为铜并沉积在铜片上,使CuSO4溶液因SO42-相对较多而带负电。这两种因素均会阻止电子从锌片流向铜片,造成电流表指针不发生指针偏转的现象。
【总结】盐桥的作用:盐桥在原电池中起导电作用,使整个装置形成闭合回路,盐桥导电利用的是阴、阳离子的定向移动,使电解质溶液保持电中性,从而使原电池能相对持续、稳定地产生电流。
思考:同学们思考一下,双液原电池的有什么缺点?我们可以如何改进?
教学目标:
(2)通过从单液原电池到双液原电池的学习认识盐桥、离子交换膜的作用,掌握原电池的工作原理、能准确判断离子移动方向,正确书写电极反应式,能设计原电池。
评价目标:
(2)通过分析单液原电池的弊端并提出改进措施,诊断并发展学生对原电池的认识进阶(宏观水平、微观水平、内涵水平)
【实验探究一】:比较单双液原电池优缺点
单液原电池虽然电流大,但是不稳定,有很大的能耗;双液原电池虽然电流稳定,但是电流又比较小,效率不高。
【思考与交流】为什么双液原电池的电流如此小?如何改进出更高效的原电池呢?
分组讨论:提出各种可能性
提示:请同学们思考,离子在两种电池的电解质溶液中的运动有何不同?
展示:单液原电池和双液原电池微观粒子运动图像
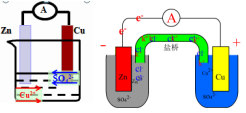
基于以上分析,同学们再讨论得出结论:盐桥的加入,使得离子通道变得又长又窄。
继续提问:那我们如何改进新的装置,能够使得电池更高效。
通过观察提示图片分析:
展示图片:三峡大坝的图片,可以U型管变为直线型盐桥

改进方案:
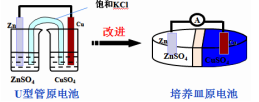
【实验探究二】提醒:没有凝胶该怎么办呢?有浸泡了KCl饱和溶液的土豆泥代替
学生组装好装置,进行测量
【思考与交流】对比U型管盐桥原电池,培养皿原电池的优缺点是什么?(从电流大小、稳定性、药品用量三个方面思考,并填写实验报告)
学生通过对比两组电池,发散思维,为后面创新改进打下基础。
教学目标:
(3)通过原电池装置优化探究过程,感受原电池的价值,了解化学在生产生活中的应用,培养可持续发展的意识,增强社会责任感,
评价目标:
(3)通过对原电池装置优化探究过程,诊断并发展学生的认识思路结构化水平(视角水平、内涵水平)和学生对化学价值的认识水平(学科和社会价值视角)。通过对学生实验操作的评价,诊断并发展学生实验操作水平。
【实验探究三】原电池的高效化创新改进
【思考与交流】培养皿原电池电流增大数倍,药品用量大,能否设计更微型化的原电池?
引导:1、滤纸既可以吸收大量溶液,作为反应池;
2在教师引导下得出创新方案2:
(1)滤纸条作为反应池;
(2)占有饱和KCl溶液滤纸当做盐桥;
学生议论纷纷,讨论得出创新方案2,并根据实验步骤进行实验操作,得出实验结论。
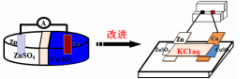
【思考与交流】是否还能够设计出更高效,微型的电池呢?
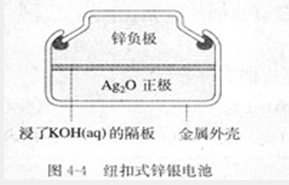
联想到纽扣电池,利用隔板或者隔膜隔开正负极以及两种电解质溶液
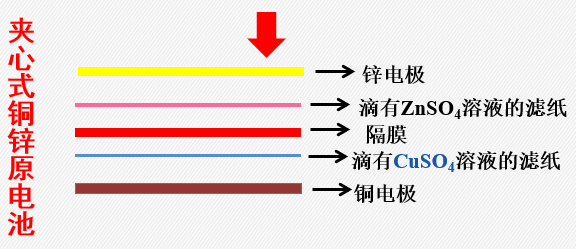
引入膜电池。
[师]通过本节课的学习,我们要理解原电池工作的原理,并且应用原电池原理解决电化学的相关问题。可以设计出更高效化、微型化的电池。
设为正确答案