- 时间点:
- 时 分 秒 当前视频时间点
- 问题:
-
- 选项一
设为正确答案
新增选项 - 选项一
- 正确跳转时间:
- 时 分 秒 同锚点时间
- 错误跳转时间:
- 时 分 秒 同锚点时间




恭喜你,回答正确~
很遗憾,回答错误~
正确答案: ,您可以



Fe2+与Fe3+的相互转化,教材以实验为载体,并利用第一章所学氧化还原反应中氧化剂和还原剂的性质及实验现象让学生掌握Fe2+与Fe3+的相互转化的过程。
之前已经学习过Fe2+与Fe3+的检验方法。以Fe2+与Fe3+的检验和第一章第三节的氧化还原反应为基础,让学生讨论如何实现Fe2+与Fe3+的相互转化,进而总结出哪些试剂可以实现Fe2+与Fe3+的相互转化。
知识目标: 通过讨论、探究,让学生掌握Fe2+与Fe3+相互转化的过程
能力目标:1、通过实验,培养学生观察,分析的能力,提升学生的总结归纳,迁移应用能力。
2、通过讨论、探究,让学生自己找出Fe2+与Fe3+相互转化的试剂,提升学生的思维能力。
情感目标:1、通过实验,可以让学生直观的观察到现象,从而引起学生的学习兴趣。
2、通过讨论、探究,可以增加同学间的沟通,让学生知道团结协作的作用。
教学重点:Fe2+与Fe3+的相互转化
教学难点: Fe2+与Fe3+的相互转化
Fe2+与Fe3+相互转化
+氧化剂
Fe2+ ![]() Fe3+
Fe3+
![]()
+还原剂
一、新课导入
苹果是常见的一种水果,但是我们应该都注意到刚切开的苹果比较透亮且带点浅绿色,但放置一段时间后,会怎么样?(此处利用多媒体-添加图片,可以让学生直观,快速地观察现象)
【学生回答】变成黄色。(此处利用多媒体-添加图片,可以让学生直观,快速地观察现象)

【教师讲述】为什么会变色?(激发学生的学习积极性)带着这个问题进入我们今天的学习。
二、新课讲解
打开课本68页,完成实验3-3。先将实验过程讲解一遍。
【实验3-3】在盛有2mL FeCl3溶液的试管中,加入少量铁粉,振荡试管。充分反应后,滴入几滴KSCN溶液,观察并记录实验现象。把上层清液倒入另一支试管中,再滴入几滴氯水,又有什么现象。(请一位同学做演示实验)。(此处利用摄像,将学生的实验操作投影到白板上,可以让更多学生更清楚的观察实验过程及现象)(学生边观察边描述实验现象)
【实验现象】加少量铁粉震荡后,溶液变成浅绿色,再加KSCN溶液不显血红色,再滴加氯水后,溶液变成血红色。(此处利用动画-擦入,可以使学生更清楚的了解实验现象)
【教师提问】FeCl3溶液为棕黄色,加入铁粉后,溶液变成浅绿色且加KSCN溶液不显血红色,说明了什么?
【学生回答】Fe3+在Fe的作用下转化成了Fe2+。
【教师讲述】请同学们写出此过程中涉及的离子方程式。(请一位同学写在黑板上,其他同学写在草稿本上)
2Fe3++ Fe = 3Fe2+ (此处利用化学方程式,使方程式的格式更规范且简便)
【教师提问】再滴加氯水后,溶液变成了血红色,又说明了什么?
【学生回答】Fe2+在氯水的作用下转化成了Fe3+。
【教师讲述】请同学们写出此过程中涉及的离子方程式。(请一位同学写在黑板上,其他同学写在草稿本上)
2Fe2++Cl2 = 2Fe3+ + 2Cl-(此处利用化学方程式,使方程式的格式更规范且简便)
【教师讲解】根据第一章的氧化还原反应,我们知道Fe是常见的还原剂,氯水中的Cl2 是常见的氧化剂。所以,由上述两个离子反应我们可以得出什么样的结论,请同学们讨论总结。
【实验结论】1:Fe3+遇到较强的还原剂时,会被还原成Fe2+;(此处利用蒙层,让学生总结归纳,提高他们的总结归纳能力)
2:Fe2+遇到较强的氧化剂时,会被氧化成Fe3+ 。(此处利用蒙层,让学生总结归纳,提高他们的总结归纳能力)
【教师讲解】那我们常见的氧化剂还原剂有哪些呢?(ppt展示一些常见的氧化剂和还原剂)(此处利用超级分类,让学生将氧化剂和还原剂进行分类,加强对常见氧化剂还原剂的记忆)
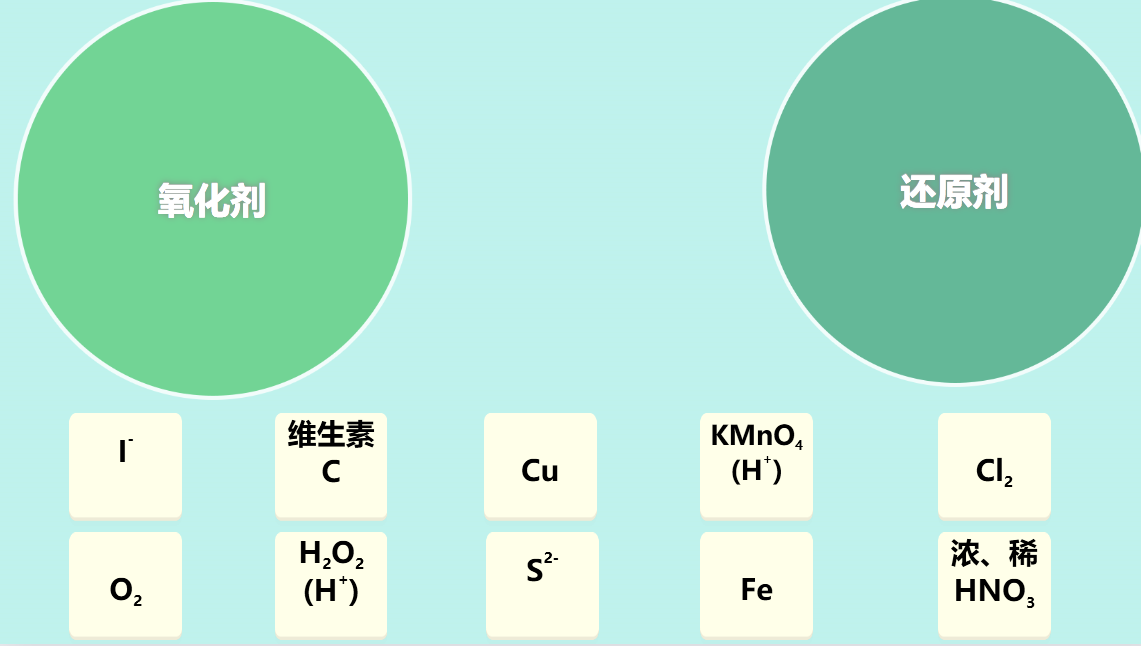
【联系生活】1:现在回到我们刚开始的问题,切开的苹果为什么会变色?
【学生回答】新切开的苹果颜色和一段时间后的颜色对比, 此现象说明O2可以将Fe2+转化为Fe3+(此处利用动画-浮现,可以让学生自己思考)
2:如果误食亚硝酸钠会使人中毒,因为亚硝酸钠会使Fe2+转化为Fe3+生成高铁血红蛋白而丧失与O2的结合能力。生死时速,假如你是医护人员,你准备怎么办?(此处利用多媒体-添加图片,增强视觉效果)
【学生回答】服用Vc

【归纳与整理】
Fe2+2Fe3+ (此处利用形状,突出重点)
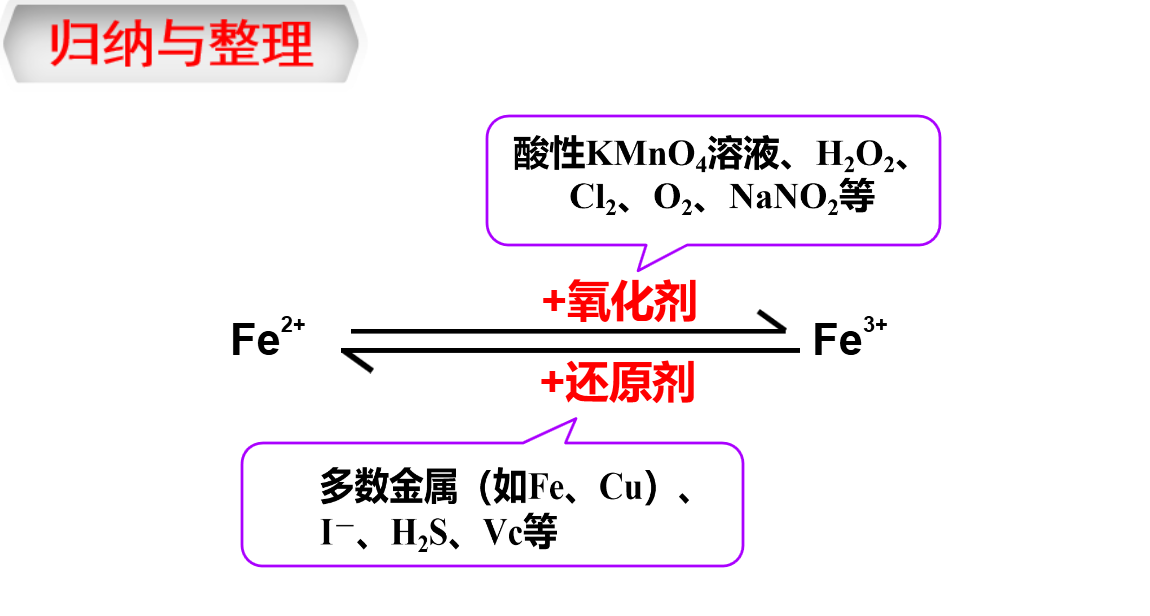
(整个过程中利用移动授课,实现了手机与电脑的同屏)
设为正确答案