- 时间点:
- 时 分 秒 当前视频时间点
- 问题:
-
- 选项一
设为正确答案
新增选项 - 选项一
- 正确跳转时间:
- 时 分 秒 同锚点时间
- 错误跳转时间:
- 时 分 秒 同锚点时间


恭喜你,回答正确~
很遗憾,回答错误~
正确答案: ,您可以



本课题是在《课题1 分子和原子》的基础上,对原子的进一步认识。在课题1学生已经树立了微观世界观,知道事物是有微观粒子分子、原子或离子构成,而且还大致了解了这些微粒的特点。还知道原子是化学变化中的最小粒子,因为化学变化中,分子可以再分,原子不能再分。而这节课就是在学生对原子已有的了解上进一步认识原子的结构,继续认识微观世界。
课件、动画视频
1.知识与技能目标
了解原子的构成;了解原子核外电子是分层排布的;初步学会分析原子结构示意图。
2.过程与方法
观察1-18号元素的原子结构示意图,归纳核外电子排布的规律
3.情感态度与价值观
进行物质是可分的辩证唯物主义观点的教育
重点:原子的结构,原子核外电子的排布
难点:原子核外电子的分层排布
自主学习法,归纳总结法,小组讨论法
分子和原子都是构成物质的微粒,它们有很多相似之处,比如(1,2,3),它们也有许多不同,但它们最大的区别是什么?(化学变化中,分子可以再分,原子不可以再分)如果去掉“化学变化”这一前提,原子是否可再分?可以分成什么呢?这得从原子的结构说起。
一、原子的构成
【拓展】原子的结构发展简史介绍。最终人们的研究结果如何呢,教材53页有给你答案。
【自主学习】阅读教材P53及表格3-1,完成黑板上的知识框架图:
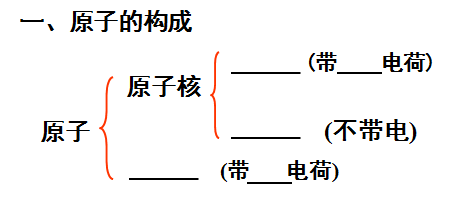
【展示】学生上台完成知识框架图
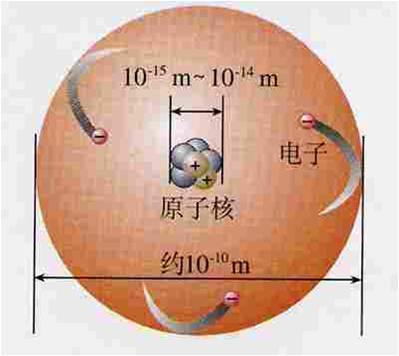
【投影】结合下图讲解,小结原子的结构
【提出问题】请学生结合表3-1,思考下列问题
1、所有的原子都是由质子、中子和核外电子构成?
2、同一种原子,质子、中子、核外电子在数量上有什么关系?
3、原子里有带电的微粒,那么原子显电性吗?为什么?
【归纳总结】1、并不是所有的原子都有中子
2、同一原子里:质子数=核电荷数=核外电荷数
3、原子里,带正电的质子和带负电的电子数量相等,但电性相反,所以整个原子不显电性。
二、原子核外电子的排布
【提出问题】原子的体积很小,如果把原子放大成一个体育场,原子核只相当于体育场中心的一只蚂蚁。电子就绕核作高速运动。氢原子的核外就一个电子绕核运动,但钠原子的核外有11个电子,这些电子的运动由是怎样的呢?会不会向地球绕太阳运动一样有固定的轨道,还是在一定的范围内运动呢?
【投影】学生观看钠原子核外电子的动画视频(视频学习)。
一些核外电子在特定范围内运动的现象就是核外电子的分层排布。
【提问】核外电子在哪个电子层上运动由什么决定?(电子的能量)
【老师】这是原子的平面结构,原子中心的红色部分代表原子核,有两个电子(用两块磁铁表示)在离核最近的电子层内运动,请同学用剩余的磁铁表示出某一时刻第二层和第三层电子层上电子的排布。
【学生】展示某一时刻第二层和第三层电子层上电子的排布。
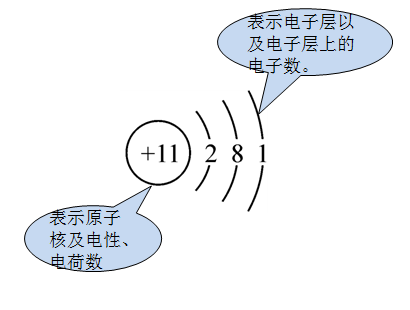
【老师】原子结构示意图可形象直观的表示核外电子的分层排,原子结构示意图与大家熟悉的WiFi图相似,我以钠原子为例,画出钠原子的原子结构示意图(如下图所示)。
【练一练】1、如图为某粒子的结构示意图,有关该粒子的说法中错误的是( )
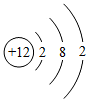
A.该粒子的原子核外有12个电子
B.该粒子原子核内有12个质子
C. 该粒子核外共有3个电子层
D.该粒子最内层电子数与最外层电子数之差为6
【提问】这是1-18号元素原子的结构示意图,出图中我们可以看出每种元素原子的核外电子排布。请同学们找一找:最内层、最外层最多能容纳的电子数分别是多少?第二层呢?你还能发现什么规律?
【交流讨论】小结:最内层最多可容纳2个电子;最外层最多可容纳8个电子(只有一层时,电子不超过2);第二层最多可容纳8个电子;
【拓展】补充:电子排布时先排满最内层,再排外层。
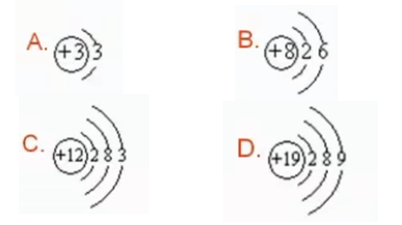
【练一练】2、下列原子结构示意图中,正确的是( )
画一画:核外有17个电子的氯原子结构示意图
原子的结构,原子核外电子的排布及规律,具体见板书
板书:

1.家庭装修材料中的有害物质会影响人体的健康。如某些花岗岩石材中就含有放射性元素氡。若一种氡原子的质子数为86,中子数为136,这种氡原子核外电子数为 ( )
A.50 B.222
C.136 D.86
2.下图为溴原子的结构示意图,则下列说法错误的( )
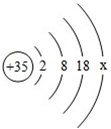
A.x=7
B.该原子的中子数一定为35
C.溴原子核内有35个质子
D.该原子的第3个电子层上有18个电子
3.下列微粒,按要求填空(填字母)
a.分子; b.原子; c.质子;
d.中子; e.原子核; f.核外电子;
(1)构成物质的微粒_____;
(2)化学变化中的最小粒子是____;
(3)原子中带正电荷的粒子是_____;
(4)不显电性的粒子是_____;
(5)在同一原子中数目相等的粒子是____;
设为正确答案