- 时间点:
- 时 分 秒 当前视频时间点
- 问题:
-
- 选项一
设为正确答案
新增选项 - 选项一
- 正确跳转时间:
- 时 分 秒 同锚点时间
- 错误跳转时间:
- 时 分 秒 同锚点时间


恭喜你,回答正确~
很遗憾,回答错误~
正确答案: ,您可以



本节包括两部分内容:氧化还原反应,氧化剂和还原剂。
教材首先设置了“思考与讨论”,以初中学过的两个化学反应为载体,引导学生从三个方面(①得氧物质、失氧物质及其发生的反应,②反应前后元素化合价的变化情况,③氧化反应或还原反应与元素化合价升降的关系)进行分析,在此基础上,得出氧化还原反应的概念,并将物质发生氧化反应或还原反应与元素化合价升降联系起来。
然后,教材以Fe与CuSO4的反应为例,将氧化还原反应的内涵从得氧、失氧扩展到反应前后有元素化合价发生变化,并说明元素化合价发生变化是氧化还原反应的重要特征。
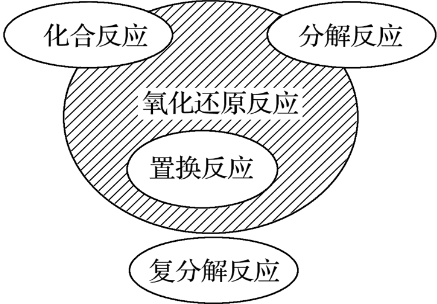
最后,教材从微观角度引导学生认识氧化还原反应的本质,这是本节的重点内容。教材以Na与Cl2、H2与Cl2的反应为例,从原子结构的角度讨论氧化还原反应中电子得失、共用电子对偏移的情况,引导学生认识氧化还原反应中一定存在着电子转移,从而形成认识氧化还原反应的微观视角。同时,教材给出4种基本类型的反应与氧化还原反应的关系示意图,将依据不同标准对化学反应进行的分类有机地联系在一起,起到了帮助学生巩固概念和提高认识的作用。
在认识氧化还原反应本质的基础上,教材从电子转移的角度定义氧化剂和还原剂,并以CuO与H2、Na与Cl2的反应为例,说明氧化剂和还原剂的关系,同时介绍了中学化学中常用的氧化剂和还原剂等。随后,教材安排了“思考与讨论”,以汽车尾气系统的催化转化器中发生的化学反应为例,引导学生从科学.技术.社会.环境(STSE)视角感受氧化还原反应的社会价值,形成“绿色化学”的理念,增强社会责任感。
本节内容的特点是概念多、抽象,理论性强。在呈现方式上,教材一方面注意初、高中的衔接、结合具体的化学反应实例,以氧化还原反应概念的发展过程为线索,即“得氧、失氧→元素化合价升降→电子转移”,从宏观视角(元素)到微观视角(电子),由表及里,环环相扣,逐步揭示氧化还原反应的本质,引导学生建构氧化还原反应的认识模型。另一方面,充分发挥氧化还原反应的社会价值,引导学生从化学的视角分析和解决实际问题,体会化学对人类文明和社会发展的促进作用。
《氧化还原反应(第一课时》学情分析
一、学生已有基础
(1) 、能从得失氧的角度判断氧化还原反应;
(2) 、已识记一些常见元素化合价;
(3) 、通过原子结构示意图知道了NaCl、 HCl的形成过程;
(4) 、初步养成了从宏观辨析和微观探析的角度来分析化学问题。
二、学生认知的关键点
(1) 、从化合价的角度认识氧化还原反应;
(2) 、从宏观辨析和微观探析的角度认识氧化还原反应的本质——电子转移;
(3) 、通过学习氧化还原的本质初步体会证据推理与模型认知。
三、学生认知的障碍点
(1) 、得到电子化合价下降,失去电子化合价上升;
(2) 、氧化剂、还原剂与电子转移的关系
四、学生认知的发展点
(1) 、通过对NaCl、 HCl的形成过程分析,初步了解电子式的用法;
(2) 、在学习氧化还原反应的过程中让学生体会到了一个理论的完善是一个长期发展的过程;
(3) 、基于证据推理与模型认知的学习,从微观视角(电子),引导学生建构氧化还原反应本质的认识模型。
1、 从宏观(化合价)角度进行分析,认识化合价的升降与氧化还原反应的关系。
2、 了解氧化还原反应概念的发展过程,体会用发展的眼光看待所学的化学知识。
3、 基于化合价变化与电子转移的相关性,从微观视角(电子),引导学生建构氧化还原反应的认识模型,初步体会证据推理与模型认知,从微观上认识氧化还原反应的本质。
4、初步理解从微观(电子得失)角度定义氧化剂与还原剂。
一、教学重点
1、从化合价的角度认识氧化还原反应。
2、从得失电子的角度定义氧化剂与还原剂。
3、从微观视角(电子),引导学生建构氧化还原反应的认识模型,从微观上认识氧化还原反应的本质。
3、通过学习氧化还原的本质初步体会证据推理与模型认知,提高学生的化学核心素养。
二 、教学难点
1、从宏观辨析和微观探析的角度认识氧化还原反应的特征(化合价的变化)和本质(电子转移)。
2、根据电子带负电,理解“得到电子化合价下降,失去电子化合价上升”。
第二节 氧化还原反应
一、定义
1.0版 有物质得氧和失氧的反应
2.0版 有元素化合价升降的反应
二、思考:什么原因导致元素的化合价发生变化?
氧化还原反应的特征:化合价升降
本质:电子转移
三、规律:
氧化剂 得到电子 化合价下降
还原剂 失去电子 化合价上升
【展示】教学目标
1、 从宏观(化合价)角度进行分析,认识化合价的升降与氧化还原反应的关系。
2、从微观视角(电子),建构氧化还原反应的认识模型,从微观上认识氧化还原反应的本质。
3、什么是氧化剂与还原剂
教师活动 |
学生活动 |
设计意图 |
【展示】燃烧 光合作用图片、文字——氧化还原反应的发现是一个漫长的过程
|
【观看】 |
使学生进入问题情境 |
教师活动 |
学生活动 |
设计意图 |
【展示】拉瓦锡 燃烧学说 【思考与讨论】 【提问】同学们发现了什么规律? 【过渡】梳理学生观点,总结规律 |
【分组讨论】从得氧、失氧的角度体验氧化还原反应
预期结论:1、氧化还原反应同时发生 2、得到氧的数目与失去氧的数目相等 |
初步体会氧化还原反应的特征 |
教师活动 |
学生活动 |
设计意图 |
【展示】弗兰克兰 化合价 【讨论】从化合价角度分析上述两个化学方程式及铁与硫酸铜的反应 【提问】这三个反应从化合价的角度来看,有什么共同点? 【板书】有元素化合价升降的反应是氧化还原反应。 【练习】共有2类练习,巩固对特征的理解和应用。 【小结】氧化还原反应的特征 【过渡 提问】什么原因导致元素化合价发生了变化?
|
【分组讨论】从得氧、失氧的角度体验氧化还原反应
【讨论】表述自己找到的规律
【巩固】从元素化合价是否变化来判断一个反应是否为氧化还原反应。 |
认识氧化还原反应的特征
初步应用氧化还原反应的特征 |
教师活动 |
学生活动 |
设计意图 |
【展示】NaCl的形成过程
【过渡】 |
【观看】从结构与性质的角度感受物质的形成过程。 |
结合结构式让学生感受物质形成过程。
初步体会“宏观辨析与微观探析”相结合的分析方法 |
教师活动 |
学生活动 |
设计意图 |
【展示】HCl的形成过程
|
【观看】体会形成共用电子对过程中化合价的变化原因。 |
初步体会“宏观辨析与微观探析”相结合的分析方法。
为以后学习离子键、共价键打下基础。 |
教师活动 |
学生活动 |
设计意图 |
【提问】有实验能证明我们上述猜想吗? 【演示实验】锌与硫酸铜溶液反应 【提问】为什么指针发生了偏转? 【过渡】梳理学生观点,总结
|
【观看】
【交流讨论】为什么指针发生了偏转? |
初步体验“模型认知与证据推理”的化学核心素养研究方法 |
一、小结:
1.所有的氧化还原反应中都存在电子转移,电子转移是氧化还原反应的本质。
2.元素化合价的变化是电子转移的外在表现,可以通过分析反应中是否有元素的化合价发生变化来判断某个反应是否属于氧化还原反应。
二、巩固练习
判断下列哪些是氧化还原反应?属于哪种基本反应类型?

小结:氧化还原反应与四大基本反应类型的关系
练习

设为正确答案